SindHosp reuniu especialistas da medicina diagnóstica, hospitais, indústria e farmácia em debate sobre consultas públicas da Anvisa
25 de novembro de 2020
Debatidas incessantemente nas últimas semanas pelos
protagonistas do setor de saúde, as Consultas Públicas 911 e 912 – sobre realização
de exames laboratoriais em qualquer serviço de saúde –, abertas pela Agência
Nacional de Vigilância Sanitária (Anvisa), foram tema de encontro virtual
promovido em 19 de novembro pelo Sindicato dos Hospitais, Clínicas e
Laboratórios do Estado de São Paulo (SindHosp). Na reunião intitulada “Só os
laboratórios estão sob ameaça?”, a Associação Brasileira de Medicina
Diagnóstica (Abramed) foi representada pelo presidente do Conselho de
Administração, Wilson Shcolnik, que defendeu o posicionamento da entidade de
que liberar a realização de exames fora dos ambientes altamente controlados dos
laboratórios aumenta o acesso, mas também aumenta o risco ao paciente.
Moderado por Francisco Balestrin e Luiz Fernando Ferrari
Neto, respectivamente presidente e vice-presidente do SindHosp, o debate também
recebeu Carlos Eduardo Gouvêa, presidente-executivo da Câmara Brasileira de
Diagnóstico Laboratorial (CBDL), Gonzalo Vecina Neto, sanitarista,
ex-presidente da Anvisa e ex-secretário municipal de Saúde; e Marcos Machado
Ferreira, presidente do Conselho Regional de Farmácia do Estado de São Paulo
(CRF-SP). O intuito do encontro foi abrir o diálogo permitindo que todos os
envolvidos tivessem voz.
Partindo do cenário da medicina diagnóstica, na ocasião
representada por Shcolnik, foi feito um breve retrospecto regulatório. O
executivo reforçou que a revisão da RDC 302 tem sido um pleito frequente do
segmento, visto que com a modernização de tantos processos que impulsionaram
novas práticas, uma atualização se fazia necessária. “A RDC 302 disciplinou o
setor de forma sensacional trazendo requisitos de gestão de qualidade para as
três fases do processo laboratorial: pré-analítica, analítica e pós-analítica.
Porém, após 15 anos, essa regulamentação não estava mais adequada aos novos
métodos adotados”, disse o presidente ao enfatizar que os profissionais do ramo
diagnóstico receberam com motivação a notícia de que finalmente a RDC seria
revisada.
Porém, a revisão da norma por meio das CPs 911 e 912
assustou o setor. “A CP 911 trata das práticas farmacêuticas após a Lei nº
13.021/2014 que dá a esses estabelecimentos o status de serviços de saúde.
Desde então, farmácias e drogarias estão se preparando para esse novo papel.
Mas, para nós, essa assistência farmacêutica estaria relacionada ao
monitoramento e uso de medicamentos. Não seria tão abrangente como estamos
vendo agora que outros serviços são também oferecidos”, explicou Shcolnik.
Um dos principais questionamentos do setor está na
capacitação dos profissionais que atuam em farmácias. “Na medicina, são mais de
50 especialidades e os médicos não estão preparados para exercer qualquer uma
delas. Eu, como médico patologista clínico, não posso fazer uma neurocirurgia.
Os profissionais que trabalham nas farmácias estão preparados para essa mudança
radical no papel desses estabelecimentos?”, questionou o executivo.
Para a Abramed, a ampliação que está sendo proposta pelas
consultas públicas gera dúvidas, pois não é adequado facilitar o acesso
colocando, em risco, a segurança dos pacientes. “A justificativa de acesso não
me parece razoável, pois o maior risco está na população. Sabemos que existem,
por exemplo, testes rápidos de altíssima qualidade que evoluíram
consideravelmente ao longo do tempo. Entretanto, sabemos também que há testes
de qualidade variável e desempenho questionável”, pontuou Shcolnik lembrando
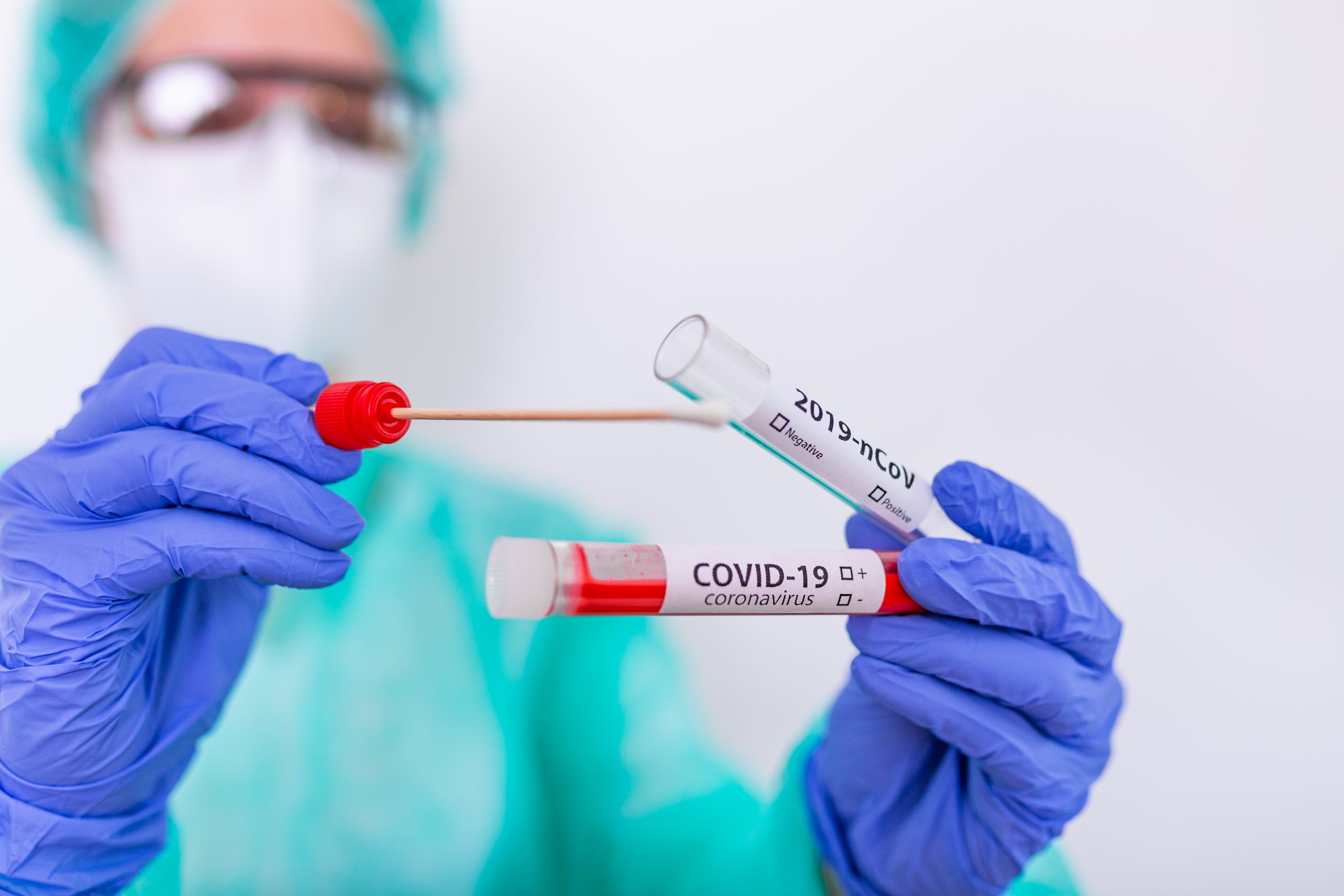
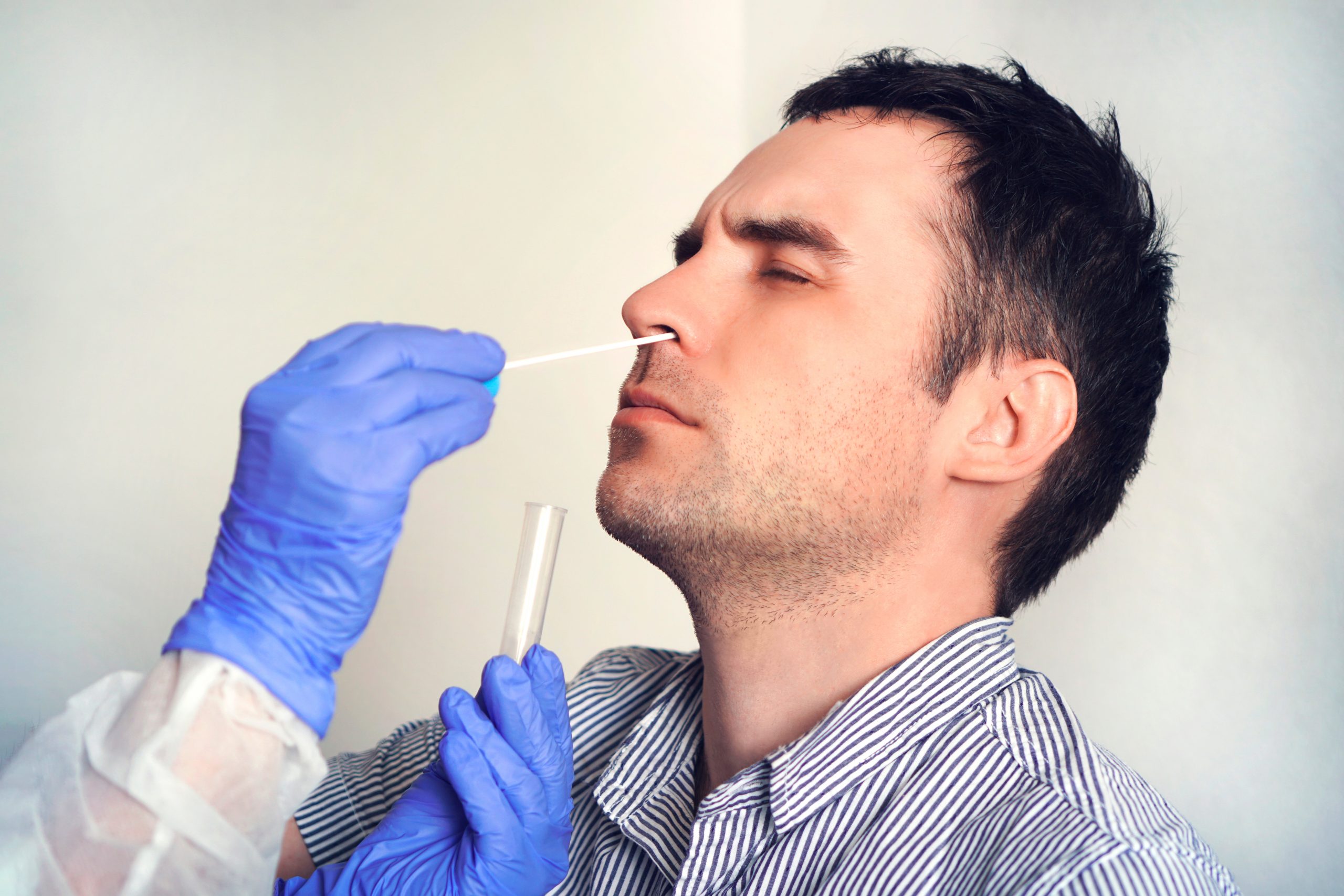
que inclusive durante a pandemia de COVID-19 a união de diversas entidades do
setor de diagnóstico e de laboratórios criou um programa de validação para
apresentar, à sociedade, quais testes para detecção do novo coronavírus eram
confiáveis.
Farmacêutico bioquímico, Ferreira trouxe a visão dos
profissionais de farmácia. “Esse debate não é tão simples de lidar”, iniciou
sua argumentação. Para ele, o caminho natural – e que já vem sendo observado no
mundo inteiro – é a farmácia avançar para outros cuidados de saúde, inclusive a
realização de exames. “Minha preocupação está em qual caminho seguir. Na CP
912, a criação do SADT-TAC (serviços de saúde que realizam atividades
relacionadas a testes de análises clínicas) permite que exames sejam feitos em
qualquer ambiente. As farmácias vieram se preparando ao longo do tempo para
isso, mas ao criar o SADT-TAC, a Anvisa permite que esses testes ocorram em
qualquer local considerado estabelecimento de saúde. Ou seja, consultório
médico, psicológico, nutricional, odontológico e muitos outros. E isso é um
problema sim quando consideramos a qualificação dos profissionais”, declarou
enfatizando que com essa abordagem perde-se o controle da situação. “Exames
sairão das mãos de profissionais qualificados, que se prepararam para tal, e
isso é preocupante demais”, completou.
Essa mudança de nomenclatura também foi um ponto de
questionamento por parte de Ferrari: “nossa estranheza está na destruição da
RDC 302 somada à mudança até do nome para SADT-TAC”, citou. Para Balestrin, a
impressão é de início de um processo que transformará as farmácias em clínicas
populares prontas para receber o cidadão não atendido pelo SUS. “Aquele que não
tem cobertura de saúde vai até uma farmácia e resolve seu problema. Mas isso é
muito insuficiente quando pensamos, de fato, na gestão de saúde do cidadão”,
falou mencionando a importância de debater a saúde baseada em valor. Já Vecina
acredita que colocar as farmácias como hubs de saúde é algo inaceitável.
“Vivemos um tempo em que existem extravagâncias que fazem mal à civilização.
Temos que entendê-las negando a possibilidade que ocorram”, declarou.
Qualidade e validação
Apresentando a perspectiva da indústria que se empenha em
fornecer kits de testes para abastecer a demanda interna e externa, Gouvêa
falou sobre a incorporação tecnológica que vem ocorrendo para otimizar os
processos produtivos e enfatizou ser necessário desmistificar as más impressões
que se instalaram após muitos testes rápidos de COVID-19 serem criticados,
justamente, por seu baixo desempenho.
“Os primeiros testes que saíram não eram bons, tinham
acabado de ser desenvolvidos. À medida em que fomos avaliando esses testes, os
fabricantes melhoraram seus processos. Nossa inovação é incremental, ou seja,
utiliza o feedback dos profissionais que estão na ponta. Tivemos, inclusive,
fabricantes que desistiram de lançar esses kits por perceber que seus produtos
não tinham qualidade e que não teriam condições de melhorá-los rapidamente”,
declarou.
Para o executivo da CBDL, o teste rápido nunca terá a mesma
sensibilidade e especificidade dos apontados como padrão ouro, mas podem
atingir um segmento da população maior, atuando como triagem. “A pessoa que
passa por esse teste e tem um resultado positivo, precisará de confirmação”,
declarou. Segundo Gouvêa, com essa ampliação proposta pelas consultas públicas,
os laboratórios serão ainda mais acessados para exames complementares, de maior
qualidade.
Vecina parte do pressuposto de que é impossível negar os
avanços do sistema. “Não podemos nos posicionar contra melhorias que promovem o
bem-estar. O que é melhor, tem que ficar”, disse. Para o especialista, os
testes rápidos podem ser realizados por diferentes profissionais de saúde,
desde que tenham sua qualidade comprovada. Para ele, o importante é não
transformar o cuidado em saúde em algo totalmente comercial.
“O consumidor, protegido pelo Código de Defesa do
Consumidor, tem direito a fazer o que bem entender, mas o produto a ele
ofertado precisa de adequada especificidade e precisa ser validado”, pontuou. A
liberação de testes rápidos para COVID-19 sem validação no começo da pandemia
foi, na opinião de Vecina, um grande erro. “A Anvisa errou, mas todo mundo
errou. O que fizemos foi fruto da nossa ignorância na ocasião. Mas agora as
coisas melhoraram e temos de olhar para o futuro”, alertou.
Impor limites é fundamental
Para Ferreira – e também para a Abramed –, é preciso
discutir a normatização definindo parâmetros assim como ocorre em outras partes
do mundo. “Quais testes laboratoriais são possíveis de serem feitos nas
farmácias? Precisamos discutir de forma mais clara”, alegou.
Vecina também concorda com a ideia de que é imprescindível
definir os limites: “temos que decidir o que pode e o que não pode ser feito em
farmácia; discutir quais testes serão liberados”.
Para encerrar a apresentação, Shcolnik pediu a todos que
jamais esqueçam que o tema central de todo esse debate é saúde. E que é preciso
sempre pensar até que ponto a liberalidade protege o cidadão. “A Anvisa foi
criada para proteger a população, mitigar os riscos. Se há um risco identificado,
é papel da Anvisa atuar. E ela tem mecanismos para isso”, encerrou.